Sepsis : une lutte de longue haleine et de nouvelles problématiques et ambitions
Cet article est issu de L'Édition n°25.
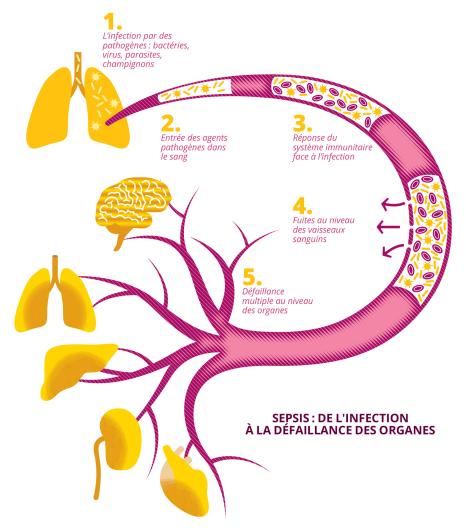
Le sepsis (ou septicémie) est une maladie résultant d’une réponse dérégulée du système immunitaire à une infection. Touchant plusieurs millions de personnes par an, enfants compris, et étant une des causes de mortalité les plus importantes dans le monde, il représente aujourd’hui un casse-tête majeur de santé publique. Comment traiter efficacement cette maladie ? Quelles solutions apporter aux patientes et aux patients ? Comment éviter les complications ? Des questions auxquelles l’Institut hospitalo-universitaire (IHU) Prometheus, associant l’Université Paris-Saclay, le CEA, l’Assistance publique – Hôpitaux de Paris (AP-HP), l’Inserm ainsi que d’autres partenaires académiques, associatifs et industriels, souhaite apporter des réponses. Officiellement lancé le 17 septembre 2024, ce premier centre mondial intégrant prévention, soin, recherche, formation et transfert technologique au sein d’un même écosystème, a pour ambition de réduire de moitié, dans les dix ans, la mortalité et les séquelles causées par le sepsis.
Définie par l’Organisation mondiale de la Santé (OMS) comme étant une des causes de décès les plus fréquentes dans le monde, le sepsis (ou septicémie) est une affection grave qui résulte d’une perte de contrôle du système inflammatoire à la suite d’une infection et qui conduit à l’atteinte des fonctions vitales de l’organisme. D’après l’organisation onusienne, elle touche chaque année près de 50 millions de personnes dans le monde (dont 45 % d’enfants de moins de cinq ans) et est responsable d’un décès sur cinq. Elle est également à l’origine de handicaps psychiques et moteurs chez un ou une survivante sur deux.
« Le sepsis est une maladie dysimmunitaire due à une première infection – bactérienne, virale, parasitaire ou fongique – à déclaration aiguë et brutale. La maladie se définit également par un potentiel évolutif sur le long terme, caractérisé par des rechutes pour environ un tiers des patientes et patients affectés une première fois, ou sous la forme de séquelles concernant des fonctions cognitives et engendrant des handicaps physiques ou le déclenchement de nouvelles maladies inflammatoires ou autoimmunes », décrit Djillali Annane, responsable de l’équipe d’étude de la réponse neuroendocrine au sepsis (SEPSIS), au sein du laboratoire Infection et inflammation (2I – Univ. Paris-Saclay/ UVSQ/Inserm). Spécialiste de cette maladie à laquelle il se consacre depuis trente ans, Djillali Annane est aujourd’hui à la tête de l’Institut hospitalo-universitaire (IHU) Prometheus, dont le but est de réduire de moitié, d’ici dix ans, la mortalité et le coût social et financier que représente le sepsis. Rien qu’en 2019, on dénombrait en France plus de 400 cas de sepsis pour 100 000 habitants, avec un coût d’hospitalisation d’environ 16 000 € par personne.
Appréhender le sepsis sous un angle nouveau
Lauréat en 2023 de l’appel à projets opéré dans le cadre du plan gouvernemental France 2030, l’IHU Prometheus réunit plus de 250 scientifiques d’une soixantaine de laboratoires, issus majoritairement de l’Université Paris-Saclay, du CEA, de l’AP-HP et de l’Inserm, ainsi que leurs partenaires académiques, associatifs et industriels, autour de la lutte contre cette maladie et le fardeau sanitaire, social et économique qu’elle représente. Intégrant des chercheurs et chercheuses, des soignantes et soignants, des patientes et patients, des institutions et partenaires privés au sein d’un écosystème de prévention, de soin, de recherche, de formation et de transfert technologique, il doit aider au développement de nouveaux tests diagnostiques et de nouveaux médicaments.
Outre des équipes de recherche déjà spécialistes du sepsis et travaillant de longue date sur cette maladie, l’IHU Prometheus en implique également de nouvelles, dont le sujet leur est plus éloigné, afin de faire émerger des innovations disruptives. « Nous réunissons des collègues dont les domaines de prédilection sont les mathématiques, la chimie, la physique, le climat, l’immunologie fondamentale, les sciences vétérinaires, etc. et qui, durant les dix prochaines années, consacreront une partie de leur temps de recherche au sepsis, en impulsant des approches originales, diverses et sans à priori », s’enthousiasme Djillali Annane. Car l’enjeu est grand : malgré des décennies de recherches abondantes, les mécanismes du dérèglement de la réponse immunitaire aux pathogènes restent encore mal connus et aucun traitement ne donne aujourd’hui entière satisfaction. Une des ambitions scientifiques de l’IHU Prometheus est notamment de mieux comprendre les interactions moléculaires et cellulaires existant entre l’organisme hôte et les pathogènes à l’origine de la progression de l’infection non compliquée vers le stade du sepsis. Une cohorte longitudinale de 10 000 patientes et patients, suivis sur dix ans, devra faciliter la compréhension du sepsis long et ses conséquences sociales et économiques.
Les corticoïdes : des premières armes pour freiner la mortalité due au sepsis
Généralement, lorsqu’un organisme est confronté à un agent pathogène (bactérie, virus, parasite, champignon, etc.), son système immunitaire déclenche une réponse adaptée circoncisant le développement de l’agent pathogène avant sa destruction et son évacuation de l’organisme. « La plupart des infections sont généralement sans grands dommages pour l’organisme », précise Djillali Annane. « Dans l’immense majorité des cas, les infections sont modérément symptomatiques et un grand nombre d’entre elles disparaît du seul fait de nos défenses naturelles. »
Il existe cependant des cas de figure où la réponse immunitaire à une infection de l’organisme se montre disproportionnée : soit elle est excessive, endommage un grand nombre de tissus et altère le fonctionnement des organes du corps humain, soit elle est insuffisante et expose au risque de surinfection. « On parle d’immunoparalysie lorsque le système immunitaire se retrouve dans un état de fragilité l’empêchant de répondre à toute nouvelle agression », décrit le professeur.
Dans leur quête de traitement contre le sepsis, Djillali Annane et son équipe démontrent, dès 1994, l’intérêt d’utiliser un traitement à base de corticoïdes sur des échelles modérées de temps et de dosage, pour diminuer la mortalité associée à la maladie. Les corticoïdes représentent un ensemble d’hormones stéroïdiennes sécrétées par les glandes surrénales de l’organisme, logées dans l’abdomen. Ils influent sur le stress, l’utilisation des sucres et les systèmes immunitaire et inflammatoire de l’organisme. « Les corticoïdes font partie de l'arsenal de défense de l'organisme : le cortisol, l’aldostérone, etc. sont fabriqués naturellement par notre organisme pour se défendre contre les agressions extérieures, y compris les agents pathogènes et infections », confirme Djillali Annane. Les corticoïdes existent également aujourd’hui sous la forme de molécules de synthèse, dont le développement remonte aux années 1950.
Utilisés à forte concentration, les corticoïdes ont un pouvoir immunosuppresseur perturbant l’activité du système immunitaire. « Nous travaillons sur le sujet de la contribution des corticoïdes à cette dérégulation, cette réponse dysimmunitaire à l’infection et synonyme de sepsis. Nous avons démontré qu’effectivement, par le biais de différents mécanismes, les agents pathogènes provoquent une altération du système de défense, comprenant les corticoïdes, et contribuent à une réponse disproportionnée de l’organisme à la menace. Fort heureusement, il est aujourd’hui possible de synthétiser des corticoïdes. Nous avons donc mené des expériences visant à utiliser les corticoïdes pour compenser cette dérégulation de l’organisme. Nous avons beaucoup travaillé sur les mécanismes moléculaires impliqués, sur des modèles animaux, cellulaires et également sur des patientes et patients, pour essayer de mieux comprendre les différentes étapes altérant cette défense de l’organisme et comment la compenser », développe Djillali Annane, véritable pionnier du traitement de la maladie par l’administration contrôlée de corticoïdes. « Nous avons été les premiers à établir qu’effectivement, une certaine modalité d’administration de la combinaison de l’hydrocortisone avec la fludrocortisone, donnée à des doses modérées sur des durées n’excédant pas sept jours, compense, au moins partiellement, l’altération ayant provoqué le sepsis », confirme le chercheur.
Une nécessaire médecine de précision
En revanche, la sensibilité de chaque être humain aux traitements et aux molécules étant très variable, Djillali Annane et son équipe travaillent depuis dix ans à identifier des « profils » de patientes et patients. « On sait en médecine qu’il est possible d’améliorer l’efficience des traitements par l’individualisation de leur administration. Cela se fait en réussissant à identifier les patientes et patients qui bénéficieront particulièrement d’un traitement, et celles et ceux qui, au contraire et pour diverses raisons, ne recevront aucun effet – ou pire, qu’il aggrave leur situation. C’est la médecine de précision. »
Pour cela, elles et ils font appel à des outils de biologie moléculaire, comme la transcriptomique (l’étude des acides ribonucléiques, ARN) ou la métabolomique (l’étude des métabolites), combinés à des outils prédictifs d’intelligence artificielle, tels que le machine learning ou le deep learning. « Nous essayons de définir des signatures, des empreintes que l’on utilisera ensuite au chevet d’une patiente ou d’un patient pour déterminer si, oui ou non, il ou elle bénéficiera d’un traitement à base de corticoïdes. D’une certaine manière, nos travaux sur la corticothérapie représentent une "preuve de concept". Maintenant que celle-ci est établie, l’IHU Prometheus a pour vocation de la déployer et d’embrasser les différentes options thérapeutiques possibles, notamment en matière d’immunothérapie », développe le médecin. « À terme, ce "profilage" sera bénéfique au-delà du sepsis, comme, par exemple, dans les cas de maladies inflammatoires ou de cancers. » En collaboration avec d’autres équipes internationales, l’équipe de Djillali Annane va d’ailleurs vérifier que ce profilage soit adaptable quel que soit le contexte socio-économique.
La médecine de précision est également au coeur de l’ambition scientifique de l’IHU Prometheus, qui va notamment chercher à valider et à commercialiser une plateforme de tests rapides afin de caractériser finement, à l’échelle de chaque individu, la réponse de l’hôte à l’infection, et des cibles thérapeutiques. Cela passera par la création d’un jumeau numérique spécifique du sepsis pour anticiper précisément la réponse de l’individu aux traitements.
Bactéries et sepsis infantile
Directrice de recherche au sein de l’équipe Pathogène, immunité, microbiote (PIMs) du laboratoire Microbiologie de l’alimentation au service de la santé (MICALIS – Univ. Paris-Saclay/INRAE), Nalini Rama Rao étudie depuis plus de vingt ans, les interactions entre les bactéries pathogènes et la réponse immunitaire de l’hôte. En particulier, elle a décrypté les mécanismes de virulence de la bactérie Bacillus cereus. « Elle est un contaminant connu de l’alimentation, mais je l’ai plutôt étudiée sous l’angle hospitalier et des facteurs de virulence : Bacillus cereus est responsable d’infections graves chez les nouveau-nés, en particulier de septicémies », détaille la chercheuse. « Pendant longtemps, les hôpitaux ne se préoccupaient pas vraiment de cette bactérie : c’était un contaminant de literie, des soignantes et soignants. J’ai tenu à montrer que c’était une véritable bactérie pathogène, avec un impact réel sur cette population cible », raconte Nalini Rama Rao, qui affiche une motivation particulière à ce que ses recherches aient un intérêt clinique. « J’ai par exemple collaboré avec des hôpitaux, dans le but de changer ensemble les procédures liées à la collecte du lait maternel, aux sondes utilisées pour nourrir les enfants prématurés, afin de réduire la présence de Bacillus cereus et donc le risque de septicémie », explique-t-elle.
Troisième cause mondiale de mortalité infantile, le sepsis est responsable chaque année du décès de plus de 300 000 nouveau-nés. La résistance des bactéries aux antibiotiques complique le traitement des infections et augmente le risque de sepsis. Nalini Rama Rao a ainsi élargi ses recherches au-delà de Bacillus cereus et étudie actuellement comment bloquer la virulence des bactéries pathogènes résistantes aux traitements actuels et à l’origine de sepsis.
Quand l’antibiorésistance s’ajoute au problème
Mais comment lutter aujourd’hui efficacement contre des agents pathogènes, alors que leur survie face aux antibiotiques censés les détruire (ou antibiorésistance) s’aggrave dans le monde entier ? « Le mécanisme des antibiotiques actuels consiste à cibler les mécanismes généraux de survie bactérien. Grossièrement, l’antibiotique va inhiber la capacité de la bactérie à survivre, dans n’importe quelle circonstance », explique Nalini Rama Rao. « C’est efficace, mais cela a un double effet délétère : cela a des répercussions sur l’ensemble des bactéries du microbiote de l’hôte, dont nous connaissons désormais l’importance, et provoque des dommages de santé collatéraux. L’autre problématique, c’est l’induction de résistance. Les bactéries mutent pour survivre et résistent de mieux en mieux aux antibiotiques initialement conçus pour les éliminer. » De nouvelles solutions thérapeutiques, qui ne participent pas à l’antibiorésistance, s’avèrent donc nécessaires.
En 2017, l’OMS publie pour la première fois une liste d’agents pathogènes pour lesquels l’antibiorésistance devient critique. En mai 2024, cette liste s’agrémente de trois nouvelles familles bactériennes. Six de ces agents pathogènes parmi les plus antibiorésistants - Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa et les espèces Enterobacter - forment l’acronyme ESKAPE. Toutes ces bactéries, et notamment Bacillus cereus, partagent une protéine en commun : la protéine Mfd (Mutation frequency decline). « Cette protéine, que j’ai initialement identifiée comme un facteur de virulence chez B. Cereus, est produite par toutes les bactéries et leur est indispensable pour résister au système immunitaire de l’hôte », explique Nalini Rama Rao. Après cette découverte, la chercheuse étudie la possibilité de cibler Mfd dans le développement de nouveaux médicaments, tout en abordant une approche sensible à l’antibiorésistance. « Plutôt que de tuer la bactérie, l’idée est de la désarmer. Mfd est une protéine utile uniquement au moment du stress immunitaire et d’une inflammation. Nous développons un composé qui bloque la protéine à ce moment précis et qui rend donc la bactérie vulnérable au système immunitaire, qui s’en débarrasse. Le microbiote n’étant pas une cible du système immunitaire, notre composé a un impact sur les bactéries pathogènes, sans toucher au microbiote. »
Une protéine universelle qui ouvre une voie
Pour Nalini Rama Rao, les études liées à cette protéine ouvrent de nouvelles perspectives : « Finalement, cette protéine est universelle : elle est conservée par toutes les bactéries. C’est là qu’est née l’idée d’étendre nos connaissances à d’autres agents pathogènes et d’autres bactéries responsables d’antibiorésistance et de septicémie. » Suite à cette véritable preuve de concept, Nalini Rama Rao et son équipe voient leur projet financé par le mécénat Santé des mutuelles AXA à hauteur d’environ un million d’euros dans le but de développer un projet de recherche préclinique et d’aboutir à la création de nouveaux médicaments. Un financement de l’Agence nationale de la recherche (ANR) est attribué à l’équipe, afin de continuer la recherche fondamentale sur le sujet. Le projet est également soutenu par l’Université Paris-Saclay, via le programme de maturation POC in Labs et la Société d’accélération du transfert de technologies (SATT) Paris-Saclay.
Le développement de nouveaux traitements, tels que de petites molécules innovantes, nanomédicaments, biothérapies et vaccins, et des stratégies modulant les microbiotes, est également un des axes forts de recherche de l’IHU Prometheus.
Convaincue par ailleurs que l’antibiorésistance est une lutte de chaque instant, à la portée de toutes et tous, Nalini Rama Rao développe des projets liés à cette thématique allant bien au-delà de la recherche. En 2019, la chercheuse s’associe à la dessinatrice Claire Fouquet et publie une bande-dessinée, Résistances croisées, qui décrit la vie de laboratoire et de l’équipe PIMs en présentant les grands enjeux de l’antibiorésistance. Trois ans plus tard, un nouveau projet de plus grande envergure voit le jour : un jeu de société coopératif, Propag’action, basé sur l’utilisation de cartes et accessible dès dix ans.
Publications :
- Pitre, T., et al. Corticosteroids in community-acquired bacterial pneumonia: a systematic review, pairwise and dose-response meta-analysis. Journal of General Internal Medicine, 38(11), 2023.
- Tran, SL. et al. An anti-virulence drug targeting the evolvability protein Mfd protects against infections with antimicrobial resistant ESKAPE pathogens. BioRxiv, 2024
- https://bd-bacterie.com/

Cet article est issu de L'Édition n°25.
L'intégralité du journal est à découvrir ici en version numérique.
Pour découvrir d'autres articles et sujets, abonnez-vous au journal L'Édition et recevez les prochains numéros :