La catalyse : l'outil d'une chimie verte
(Cet article est issu de L'Édition n°23).
Par l’utilisation d’une substance (appelée le catalyseur) ne subissant pas ou le moins possible de transformations, la catalyse ouvre la voie à l’accélération voire à la sélectivité de réactions chimiques en tous genres. Observée depuis des millénaires, la catalyse est aujourd’hui un des piliers de la pratique d’une chimie soutenable, moins consommatrice et moins énergivore. Tour d’horizon des pratiques liées à cette démarche au sein de l’Université Paris-Saclay.
Au cours d’une réaction chimique, la catalyse est utilisée pour accélérer ou favoriser une voie de synthèse particulière de ladite réaction. À l’aide d’un catalyseur, il est possible de consommer moins de réactifs chimiques ou d’obtenir un produit chimique d’intérêt en plus grandes quantités. Le second avantage de la catalyse réside généralement dans la réutilisation du catalyseur après réaction : celui-ci n’est pas consommé. C’est en ce sens que la catalyse et ses nombreuses voies constituent un véritable pilier de la pratique d’une chimie soutenable et respectueuse de l’environnement. Le 23 novembre 2023, les chimistes de l’Université Paris-Saclay se sont réunis lors de la journée scientifique annuelle de la Graduate school (GS) Chimie de l’Université, portant sur les enjeux d’une chimie soutenable et de l’avenir de la chimie catalytique.
Depuis des millénaires, les êtres humains observent tous types de catalyse. Il faut cependant attendre 1835 pour que le chimiste suédois Jöns Jacob Berzelius appose le premier le terme de catalyse sur ce phénomène. Dans son rapport annuel de cette même année, le chimiste écrit : « Il est donc prouvé que beaucoup de substances simples ou composées, solides ou dissoutes, possèdent la faculté d'exercer sur des corps composés une influence essentiellement distincte de l'affinité chimique, influence qui consiste à produire un déplacement et un autre arrangement de leurs éléments, sans y participer directement ou nécessairement, à l'exception de quelques cas spéciaux. » Près de deux siècles après cette première définition, la catalyse est devenue un pilier de la chimie moderne et il existe une multitude de types de catalyses différentes et tout autant de disciplines nouvelles : la catalyse par molécules organiques ou éléments métalliques, la photocatalyse (induite par la lumière), la biocatalyse (inspirée par les phénomènes naturels), etc.
Explorer le vivant
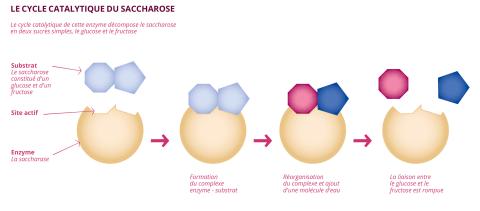
Carine Vergne et Anne Zaparucha sont toutes les deux membres de l’unité mixte de recherche Génomique métabolique (GM – Univ. Paris-Saclay, Univ. Évry, CNRS, CEA). Depuis plus de quinze ans, les deux scientifiques étudient une multitude de réactions chimiques et cherchent à développer de nouvelles voies biocatalytiques pour la synthèse de ces réactions, à l’aide d’enzymes, les protéines aux fonctions catalytiques présentes dans la nature. « La biocatalyse, c’est l’utilisation d’enzymes, communément appelées les catalyseurs du vivant, en chimie organique, présente Anne Zaparucha. De façon universelle, les organismes vivants sont le théâtre de tout un ensemble de réactions, se succédant les unes aux autres, appelé le métabolisme. Chacune de ces réactions est catalysée par une enzyme correspondante. » Par promiscuité, l’enzyme correspondant à une réaction précise du métabolisme d’un organisme vivant est utilisable au cours de la synthèse d’un autre composé, pourvu que le processus de synthèse et le produit obtenu soient similaires à la réaction métabolique. « C’est sur cette propriété de promiscuité que se base la biocatalyse. Une enzyme réagit sur son substrat métabolique, mais également sur d’autres substrats qui lui sont généralement proches », explique Anne Zaparucha. C’est donc cette propriété de promiscuité des enzymes qui rend possible la biocatalyse. « Par ailleurs, nous possédons désormais un panel d’outils absolument extraordinaire afin de modifier les enzymes à souhait. » En 2018, la chercheuse américaine Frances Arnold a été récompensée du prix Nobel de chimie pour ses travaux d’évolution dirigée des enzymes.
Depuis 2008, Carine Vergne et Anne Zaparucha enquêtent, à la découverte d’activités, de combinaisons de réactions chimiques et d’enzymes d’intérêt. « Concrètement, nous nous intéressons à une réaction en particulier, et nous cherchons ensuite les enzymes capables de catalyser cette réaction. Par ailleurs, nous ciblons de préférence les réactions pour lesquelles trouver une alternative biocatalytique a un intérêt, soit économique car la réaction est très pratiquée, soit au contraire car la réaction ciblée est peu pratiquée de par la complexité de son exécution », détaille Carine Vergne.
Oxydation, halogénation, hydroxylation, etc. : nombreuses sont les réactions qui intéressent les deux chercheuses ; mais l’amination réductrice est de loin la plus renommée. « Généralement, nous commençons nos travaux par de la bibliographie, notamment des lectures d’élucidation de voies de biosynthèse. Notre tâche est alors de trouver les enzymes idéales à implémenter à ces réactions. Ce n’est pas la seule réaction sur laquelle nous travaillons, mais l’amination réductrice reste l’un des projets phares de notre laboratoire, notamment en raison du nombre de publications sur le sujet. C’est une réaction très populaire », explique Carine Vergne. « C’est une réaction d’une très haute importance en chimie. Son champ d’application est tout à fait extraordinaire, puisque deux tiers des composés d’activité thérapeutique intègrent aujourd’hui une fonction amine dans leur structure », abonde Anne Zaparucha. De l’amination réductrice résulte l’ajout d’un groupement amine (notamment composé d’un atome d’azote) à une molécule organique.
Apporter de la diversité
Au fur et à mesure des activités du laboratoire, les deux chercheuses et leurs collègues ont participé à la constitution d’une véritable bibliothèque d’enzymes et de leurs variations. Une collection à leur disposition mais également profitable au reste de la communauté de biocatalyse. « Par rapport à d’autres équipes recherchant d’autres biocatalyseurs, nous essayons de choisir des activités où les enzymes utilisées sont peu étudiées ou leurs variations peu connues. Notre particularité réside dans notre souhait d’apporter de la diversité, par rapport à une connaissance bibliographique établie des enzymes. Ce que l’on observe dans le domaine de la biocatalyse, c’est un potentiel manque de diversité de portfolios d’enzymes disponibles », détaille Carine Vergne. « C’est cette exploration de la biodiversité qui fait notre force », assure Anne Zaparucha. « C’est d’ailleurs essentiel à notre discipline. Contrairement à la catalyse de chimie conventionnelle, où un catalyseur possède souvent une "couverture" assez large, une enzyme est active sur une poignée de produits au grand maximum. Donc, pour couvrir une grande diversité de substrats, nous devons avoir à notre portée une grande diversité d’enzymes. Voilà notre force : nous préférons découvrir de nouvelles enzymes plutôt que d’en modifier une déjà répertoriée. Et à chaque fois, c’est une diversité amenée à la communauté. »
L'unité Génomique métabolique fait partie du Genoscope, le centre national de séquençage français. C’est grâce au laboratoire de séquençage génomique et à des équipes spécialistes de bioinformatique que sont rendues possibles les explorations d’Anne Zaparucha, de Carine Vergne et de leurs collègues. « Nous nous servons de ce partenariat avec le Genoscope et de l’expertise en bio-informatique de ces équipes pour effectuer nos recherches. Nous partons d’une séquence d’enzymes connue et répertoriée dans la bibliographie pour catalyser la réaction à laquelle nous nous intéressons. Grâce au Genoscope, nous cherchons dans la biodiversité des séquences homologues, répondant à plus ou moins de critères de similarité. Le but est ensuite de produire ces séquences et les tester au sein de notre réaction initialement choisie, comme des chimistes "classiques". Viennent ensuite une phase d’analyse des résultats et produits obtenus, et une phase d’optimisation des conditions de réaction », détaille Carine Vergne.
Porphyrine, MOF et photocatalyse : un procédé novateur de synthèse du formiate
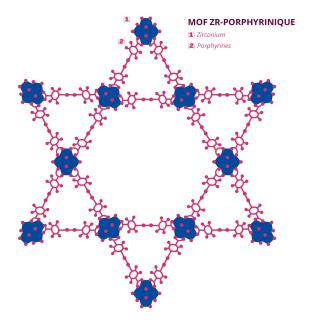
Au sein de l’Institut Lavoisier de Versailles (ILV – Univ. Paris-Saclay, UVSQ, CNRS), Anne Dolbecq et Pierre Mialane s’intéressent à la réduction, en présence de lumière visible, du dioxyde de carbone (CO2) en formiate (HCO2-), un réactif chimique utilisé dans de nombreux processus industriels. À cette fin, les deux scientifiques ont sélectionné comme catalyseur un matériau constitué d’un réseau métallo-organique porphyrinique.
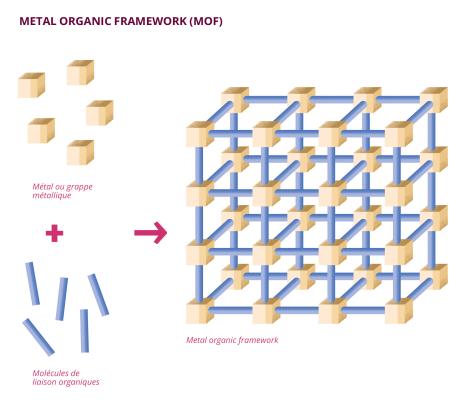
La porphyrine est une molécule organique cyclique colorée. Les réseaux métallo-organiques (metal-organic frameworks - MOF) sont des solides cristallisés composées de clusters ou d’ions métalliques reliés par des ligants organiques (principalement du carbone). Leur structure poreuse rend ces matériaux particulièrement intéressants en catalyse. En outre, il est possible pour les MOFs de « capturer » des molécules de petite taille, telles que le dioxyde de carbone. En l’occurrence, le MOF porphyrinique étudié par Anne Dolbecq et Pierre Mialane absorbe non seulement le CO2 mais celui-ci est également fixé au matériau grâce aux ions zirconium contenus dans celui-ci. C’est ensuite à l’aide d’une espèce chimique spécifique, la triéthanolamine (TEOA) et de l’usage de rayons lumineux que le dioxyde de carbone est réduit en formiate. « La porphyrine, après absorption de lumière visible, est placée dans un état excité – elle possède plus d’énergie que nécessaire, explique Pierre Mialane. Une fois excitée, la porphyrine va créer, à partir de la TEOA, une espèce radicalaire dite donneuse d’électrons sacrificielle. C’est ensuite cette espèce qui va réduire le dioxyde de carbone en formiate. » Cette réaction est décrite comme étant photocatalytique puisque c’est l’irradiation par des rayons lumineux qui déclenche le processus complexe menant à la synthèse du formiate. « Nous utilisons le caractère photosensible de la porphyrine contenue dans notre MOF pour déclencher un transfert d’électrons et ainsi engendrer la réduction du dioxyde de carbone en formiate. Les porphyrines sont connues depuis longtemps comme des espèces photosensibles, et elles jouent donc le rôle d’"antenne" dans notre MOF », détaille Anne Dolbecq. Une fois la réaction effectuée, le MOF est réutilisable plusieurs fois.
Voilà plus de cinq ans qu’Anne Dolbecq et Pierre Mialane étudient ce MOF composé de porphyrine et de zirconium. D’autant plus que depuis leur découverte dans les années 1990, l’ILV est un véritable bastion des MOFs. « Une famille de MOFs, les MIL (pour Matériaux Institut Lavoisier), est d’ailleurs originaire du laboratoire », précisent les deux scientifiques. En revanche, le MOF porphyrinique au zirconium étudié par les deux chimistes n’a lui pas été conçu dans les laboratoires de l’ILV. « Nous n’avons pas synthétisé les premiers ce MOF, il existait déjà dans la littérature. Tout comme le caractère photosensible de la porphyrine, déjà mis en évidence auparavant. En revanche, les mécanismes de réduction du CO2, très complexes, et le rôle du TEOA étaient très flous », se souvient Anne Dolbecq.
Les deux scientifiques sont à l’origine des spécialistes des polyoxométallates (POMs), des oxydes moléculaires menant par exemple à l’oxydation catalytique de l’eau. Aujourd’hui, leur nouvelle expertise des MOFs et de la réduction du dioxyde de carbone par photocatalyse leur ouvre de nouvelles voies. « Imaginez : allier un POM oxydant l’eau et fournissant des électrons pour réduire du dioxyde de carbone grâce à notre MOF. Cela conduirait à la synthèse de formiate par réduction de dioxyde de carbone en se servant de molécules d’eau. Plus de TEOA, et un mécanisme plus " joli " et plus propre », commente Pierre Mialane. « À l’avenir, on pourrait imaginer placer des dispositifs sur les cheminées d’usine rejetant du dioxyde de carbone et de la vapeur d’eau pour former du formiate », ajoute Anne Dolbecq.
Comment conduire une catalyse plus écologique ?
Parmi toutes les techniques de catalyse existantes, la plus populaire est sans doute la catalyse organométallique, faisant intervenir un complexe composé d’une structure organique et d’un métal. Particulièrement pratiquée, la catalyse au palladium est le sujet de recherche des chercheurs japonais Ei-ichi Negishi, Akira Suzuki et du chercheur américain Richard Heck, tous trois récompensés du prix Nobel de chimie 2010. Si l’efficacité du palladium en tant que catalyseur n’est aujourd’hui plus à prouver, son utilisation massive fait débat. « Concrètement, c’est un élément qui coûte cher et dont les réserves mondiales commencent à s’amenuiser », résume Christine Tran, maîtresse de conférences et chercheuse au sein du laboratoire Biomolécules : conception, isolement, synthèse (BioCIS - Univ. Paris-Saclay, CNRS). « Le palladium et d’autres métaux catalyseurs sont aujourd’hui utilisés à très grande échelle, notamment en industrie pharmaceutique. Le sujet d’une alternative à ces métaux est d’actualité. En tant que chimistes, notre rôle est aujourd’hui de trouver de nouveaux catalyseurs plus éco-compatibles. Par exemple, je développe actuellement une thématique de recherche focalisée sur la photocatalyse, une catalyse plus propre et plus facile d’accès : avec l’utilisation de la lumière comme catalyseur, nous essayons de viser des réactions en conditions douces : pas de chauffage drastique, pas de manipulations délicates, d’outils encombrants comme des boîtes à gants, etc. », complète la chimiste.
Au sein de BioCIS, Christine Tran souhaite développer de nouvelles stratégies éco-compatibles de chimie médicinale. Elle a ainsi établi une nouvelle méthode, avec une catalyse au fer, pour la synthèse de composés hétérocycliques, tels que des indoles ou des dihydrobenzocarbazoles, présentant des propriétés antifongiques. « À mon échelle, l’éco-conception débute notamment avec le choix du catalyseur et du solvant utilisé pour les synthèses, raconte la chercheuse. Je pense aussi, ensuite, à la manière avec laquelle je vais isoler mon produit final : par exemple, l’utilisation d’une colonne de silice pour purifier un produit est contournable, au vu de la toxicité de la silice, au profit par exemple d’une recristallisation. »
Références
- Ducrot L. et al, Expanding the Substrate Scope of Native Amine Dehydrogenases through In Silico Structural Exploration and Targeted Protein Engineering, ChemCatChem, Vol. 14, Issue 22, 2022.
- Benseghir Y. et al, Unveiling the mechanism of the photocatalytic reduction of CO2 to formate promoted by porphyrinic Zr-based metal–organic frameworks, J. Mater. Chem. A, 2022.
- Tran C. et al., Iron-catalyzed reductive cyclization of nitroarenes: Synthesis of aza-heterocycles and DFT calculations, Chinese Chemical Letters, Volume 34, Issue 3, 2023.
Cet article est issu de L'Édition n°23.
L'intégralité du journal est à découvrir ici en version numérique.
Abonnez-vous pour ne manquer aucun numéro.